公司电话:0769-85602287 投诉建议:150-1483-7000 邮箱:yinso2@163.com 地址:东莞市大岭山镇梅林路59号
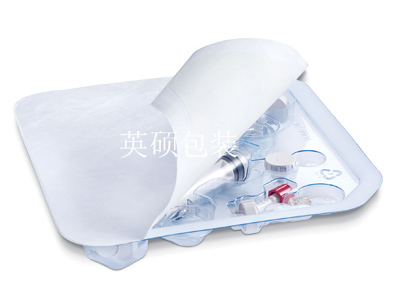
无菌医疗器械包装的材料应如何识别?
来源:英硕包装 发布时间:2018-08-31 点击量:3404
在选择无菌医疗器械包装定制之前,我们首先要对材料质量有一定了解,市场鱼目混杂,无菌医疗器械包装的材料该如何选择呢?

真正意义上,属于医用级别的材质方属于PETG材质,但并不是所有PETG的材料都适用于医用,其价格也是相差甚远,级别不能同等论处。
包装的选择会影响到对器械的保护;灭菌效果;无菌保持;无菌打开和使用等诸多方面,是非常重要的一项工作,我们应至少从以下十个方面考虑
1. 微生物屏障;
2. 生物相容性和毒理学特性;
3. 物理和化学特性;
4. 与预期灭菌过程的适应性;
5. 与包裹或密封过程的适应性;
6. 灭菌前产品的货架寿命;
7. 灭菌后无菌屏障系统的无菌保持期;
8. 运输和贮存;
9. 和被包装的器械的相容性;
10. 与标签系统的适应性。
而要满足以上要求,现目前全球只有两家PETG原料能够实现,即 美国伊士曼和韩国SK。现国内PETG原料技术还没有一家能够与之抗衡。
摘取 ISO11607-1-最终灭菌医疗器械的包装-第1部分
5.1.5应了解所有材料特别是回收材料的来源、历史和可追溯性,并加以控制,以确保最终产品持续符合本标准的要求。
注: 使用当今的工业生产技术,除生产回料以外的回收材料,不可能很好地控制使其安全地用于无菌医疗器械包装。
5.1.6 应评价下列特性:
a) 微生物屏障;
b) 生物性容性和毒理学特性;
注:这通常用来约束材料与器械的接触。ISO 10993-1给出了生物学相容性指南。宜评价灭菌对生物相容性的影响。
c) 物理和化学特性;
d) 与成型和密封过程的适应性;
e) 与预期灭菌过程的适应性;
f) 灭菌前和灭菌后的贮存寿命限度。
对此,英硕包装秉承以质量安全为核心的经营理念,无菌医疗器械包装所用材料在下游供应商提供整套生物性资料以外,并联系第三方权威检测机构分别对美国伊士曼和韩国SK材料进行检测并通过试验。
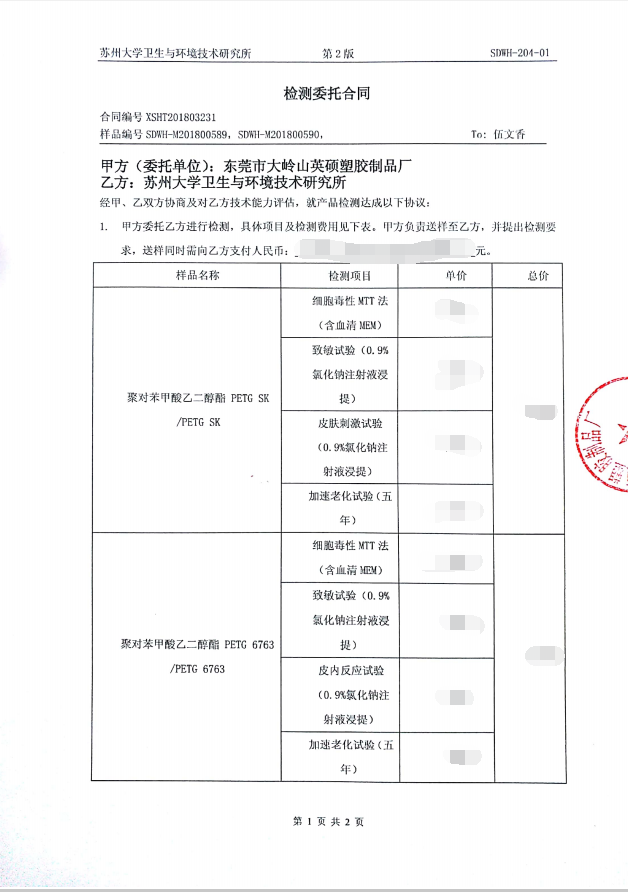
注:所有原材料报告均合作后提供,如需咨询专业知识或有合作意向请随时联系。
东莞市大岭山英硕塑胶制品厂十多年专注无菌吸塑包装,主要生产销售医疗器械吸塑包装,无菌医疗器械包装、吸塑托盘、吸塑泡罩。公司通过ISO13485认证,万级洁净车间,吸塑盒在出货前均会通过初始污染菌和不溶性微粒检测,原材料可提供生物相容性、灭菌适应性及耐老化测试等。确保安全、有效的无菌屏障系统,欢迎来电咨询0769-85602287.
责任编辑——英硕包装
版权所有www.yinsobz.com 转载请注明出处
你可能还会对这篇文章感兴趣:无菌医疗器械包装法律法规的发展历程简述
相关产品
热点资讯
- 英硕医用包装|新春开工启新程,安全护航再出发!2025-02-06
- 【英硕包装】2025 年春节放假通知2025-02-06
- 不同维度来了解医用吸塑盒与普通吸塑盒的差别2022-02-17
- 影响灭菌医疗器械包装环氧乙烷灭菌效果的因素2021-10-30
- 最终灭菌医疗器械包装常用系列标准参考2021-08-02
- 医用硬质吸塑盒的材质选择简述2021-07-20
- 无菌包装材料的评估项目及测试方法参考2021-07-17
- 影响医疗器械货架有效期的因素2021-07-17