公司电话:0769-85602287 投诉建议:150-1483-7000 邮箱:yinso2@163.com 地址:东莞市大岭山镇梅林路59号
生物相容性两大原则与评价标准
来源:英硕包装 发布时间:2019-04-20 点击量:1790
一、生物安全性原则
1、目的在于消除生物材料对人体器官的破坏性,比如细胞毒性和致癌性??
2、生物材料对于宿主是异物.在体内必定会产生某种应答或出现排异现象。生物材料如果要成功.至少要使发生的反应被宿主接受,不产生有害作用。因此要对生物材料进行生物安全性评价,即生物学评价。
二、生物功能性准则?
1、是指其在特殊应用中“能够激发宿主恰当地应答”的能力。??
2、随着对生物材料生物相容性的深入研究,人们发现不仅要对生物材料的毒副作用要进行评价,还要进一步评价生物材料对生物功能的影响。
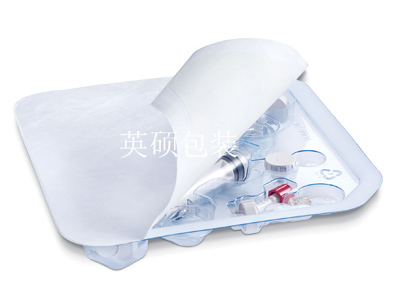
评价材料的生物相容性遵循生物安全性和生物功能性两个原则,既要求生物材料具有很低的毒性,同时要求生物材料在特定的应用中能够恰当地激发机体相应的功能。常见的医疗器械吸塑包装材料有AEET与PETG,其中PETG在医疗器械包装行业运用最为广泛,目前主要知名厂家有两家,分别为美国的伊斯曼与韩国的SK。生物相容性的评价主要参考国际标准化组织(International Standards Organization,ISO)10993和国家标准GB/T16886的要求,通过一系列体外、体内实验来进行。

体内的免疫反应和组织修复过程十分复杂,通过一种细胞或组织确定某种材料的生物相容性是不够的。评价和分析某种材料的生物形容性要明确三个关键点:第一,没有一种材料是完全的惰性材料;第二,生物相容性是一个动态的过程,不是静止不变的;第三,生物相容性不单纯是材料本身的性质,而是材料与机体环境相互作用的结果。
东莞市大岭山英硕塑胶制品厂,专注吸塑包装十余年,“质”为医疗器械包装而生,十多年专注无菌吸塑包装,主要生产销售医疗器械吸塑包装,医用吸塑盒、吸塑托盘、吸塑泡罩。公司通过ISO13485认证,万级洁净车间,吸塑盒在出货前均会通过初始污染菌和不溶性微粒检测,原材料可提供生物相容性、灭菌适应性及耐老化测试等。确保安全、有效的无菌屏障系统,欢迎来电咨询0769-85602287。
文章出自专业医疗器械吸塑生产厂家——东莞市大岭山英硕塑胶制品厂(公司网址:www.yinsobz.com)转载请注明出处!
英硕包装专注医疗器械吸塑包装,致力于服务各大医疗器械厂家及医药制品公司。公司拥有ISO Class 7万级洁净车间,全面通过ISO13485:2016。想要更进一步了解医用吸塑盒可致电:400-998-2901或0769-85602287。英硕包装将竭诚为您服务!
相关产品
热点资讯
- 英硕医用包装|新春开工启新程,安全护航再出发!2025-02-06
- 【英硕包装】2025 年春节放假通知2025-02-06
- 不同维度来了解医用吸塑盒与普通吸塑盒的差别2022-02-17
- 影响灭菌医疗器械包装环氧乙烷灭菌效果的因素2021-10-30
- 最终灭菌医疗器械包装常用系列标准参考2021-08-02
- 医用硬质吸塑盒的材质选择简述2021-07-20
- 无菌包装材料的评估项目及测试方法参考2021-07-17
- 影响医疗器械货架有效期的因素2021-07-17