公司电话:0769-85602287 投诉建议:150-1483-7000 邮箱:yinso2@163.com 地址:东莞市大岭山镇梅林路59号
最终医疗器械包装评审需注意些什么?
来源:英硕包装 发布时间:2021-05-16 点击量:758
美国FDA缺陷确认研究表明超过50%的涉及无菌医疗器械的召回事件中都与医疗器械包装的质量相关。在我们日常注册审评及注册查检中发现,很多生产企业普遍存在对最终医疗器械包装重视程度不够、理解不够的现象。比如:别人用什么包装我们就用什么包装,不清楚如何选择相适应的材料,如果开展评价,具体需要开展哪些项目等。

以下英硕包装小编整理了几点在包装评审过程中需注意的事项,仅供参考。
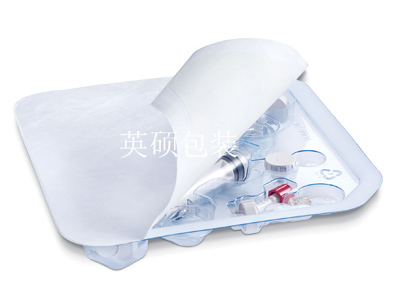
1. 无菌屏障系统(医疗器械初包装)材料的评价:
物理、化学性能、生物相容性、与器械的相互作用等。
2. 初包装的性能评价:
密封连续性、封口宽度、封口强度、包装完整性、封口剥开无落屑等。灭菌前后都应进行评价。
3. 初包装过程确认报告:
包括设备过程的IQ,OQ,PQ。应明确封口的工艺参数(如温度、压力及时间等)
4. 初包装有效期验证:
一般加速或实时老化均认可。若加速老化与实时老化验证不一致时,应以实时老化验证为准。
5. 初包装运输模拟评价:
一般应包括运输、震动、跌落测试等。
最后切记,与最终灭菌医疗器械的使用表面直接接触、不需清洁即使用的初包装材料,其生产环境洁净度的等级应当遵循与产品生产环境同等级的原则。
相关产品
热点资讯
- 英硕医用包装|新春开工启新程,安全护航再出发!2025-02-06
- 【英硕包装】2025 年春节放假通知2025-02-06
- 不同维度来了解医用吸塑盒与普通吸塑盒的差别2022-02-17
- 影响灭菌医疗器械包装环氧乙烷灭菌效果的因素2021-10-30
- 最终灭菌医疗器械包装常用系列标准参考2021-08-02
- 医用硬质吸塑盒的材质选择简述2021-07-20
- 无菌包装材料的评估项目及测试方法参考2021-07-17
- 影响医疗器械货架有效期的因素2021-07-17