公司电话:0769-85602287 投诉建议:150-1483-7000 邮箱:yinso2@163.com 地址:东莞市大岭山镇梅林路59号
医疗器械包装生物相容性和毒理学性能检测详解
来源:英硕包装 发布时间:2019-01-12 点击量:1530
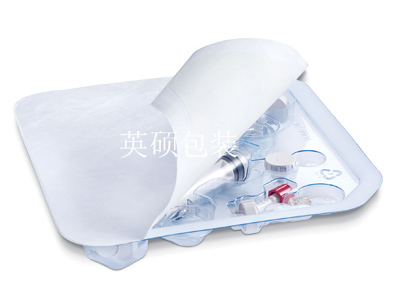
医疗器械包装的生物相容性和毒理学性能应按照ISO10993进行验证,ISO10993有16个标准,内容非常多。其中ISO10993《医疗器械的生物学评价》第7部分——环氧乙烷灭菌残留量和ISO10990《医疗器械的生物评定》第10部分——刺激与持续型过敏症试验是FDA关于这类产品的要求;但是在欧洲根据纸张的一般特性规定了几项化学检测,(例如:甲醛,镀铝联苯,五氯苯酚,纸张杀菌剂的迁移等),可以使问题更加简化,操作性更强。

医疗器械厂家可以通过标准提供的方法进行检测以及从医疗器械包装供应方处获得证书,对包装材料大多数方面进行系统的考虑。有一种情况是例外的,如果医疗器械包装材料和医疗器械之间有任何互相影响,最好由医疗器械的生产厂家予以确定。
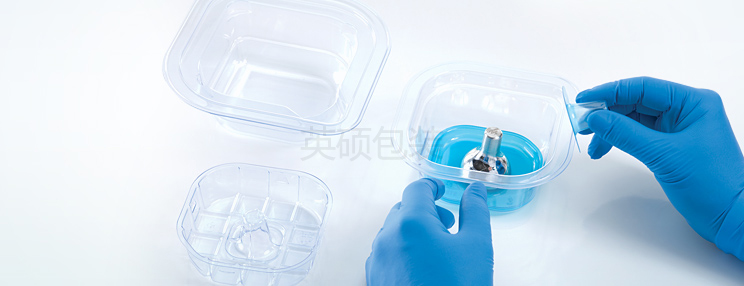

另外,还有一项可能相关的医疗器械包装安全考虑事项,即随着时间的流逝,从包装材料中溶解带出的可萃出物,有可能对医疗器械或环境造成污染。据ASTM D4754,采用FDA迁移测试槽对塑料材料进行双侧液体萃取的标准试验方法可用于材料可萃出物的测试。最终,医疗器械包装材料必须无毒。
文章出自专业医疗器械吸塑生产厂家——东莞市大岭山英硕塑胶制品厂(公司网址:www.yinsobz.com)转载请注明出处!
英硕包装专注医疗器械吸塑包装,致力于服务各大医疗器械厂家及医药制品公司。公司拥有ISO Class 7万级洁净车间,全面通过ISO13485:2016。想要更进一步了解医用吸塑盒可致电:400-998-2901或0769-85602287。英硕包装将竭诚为您服务!
相关产品
热点资讯
- 英硕医用包装|新春开工启新程,安全护航再出发!2025-02-06
- 【英硕包装】2025 年春节放假通知2025-02-06
- 不同维度来了解医用吸塑盒与普通吸塑盒的差别2022-02-17
- 影响灭菌医疗器械包装环氧乙烷灭菌效果的因素2021-10-30
- 最终灭菌医疗器械包装常用系列标准参考2021-08-02
- 医用硬质吸塑盒的材质选择简述2021-07-20
- 无菌包装材料的评估项目及测试方法参考2021-07-17
- 影响医疗器械货架有效期的因素2021-07-17