公司电话:0769-85602287 投诉建议:150-1483-7000 邮箱:yinso2@163.com 地址:东莞市大岭山镇梅林路59号
划重点!最终灭菌器械的包装评价
来源:英硕包装 发布时间:2019-07-13 点击量:1238
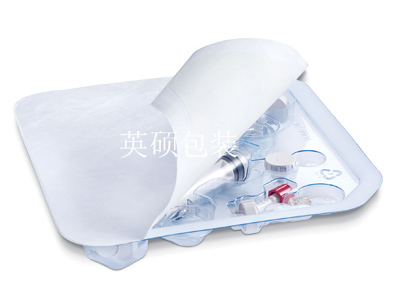
无菌医疗器械包装的研发和设计是一项非常严谨系统性的工作,所使用的包装材料的选择更是重中之重。无菌医疗器械对包装材料的选择更应结合预期的内包装实物进行全面的评价。根据ISO11607《最终灭菌器械的包装》法规要求,以下英硕小编整理了相关重点,供大家参考。
1. 微生物屏障能力
对于最终灭菌器械而言,无菌性不能被保障是严重不合格事件上。无菌包装应具有维护产品在一定有效期的基本能力。评价微生物屏障能力的方法分成两类:1. 适用于不透性材料的方法可采用ISO5636.5:2003中规定的葛尔莱法、GB/T458:2008肖波尔法),这类的包装材料常见英硕包装生产的吸塑盒所使用到的塑料,如PETG、APET等。2.适用于透气包装可采用(YY/T0681.10透气包装材料微生物屏障试验、ISO11607.1中以0.45微米为参考值进行孔径测定评价方法。

2. 生物相容性和毒理学特性要求
考虑到最终灭菌器械包装材料与医疗器械直接接触,有关生物相容性必须得到相关满足。参考GB/T 16886.1的要求,通常选择按照表面器械的生物学评价项目来进行包装材料的生物学评价是一个可接受的选择。参考ISO10993的相关检测方法,在对包装材料进行评价前应经过至少和器械一样的灭菌工艺。最终灭菌器械包装中存在液体时,应对包装溶出物质进行评价。
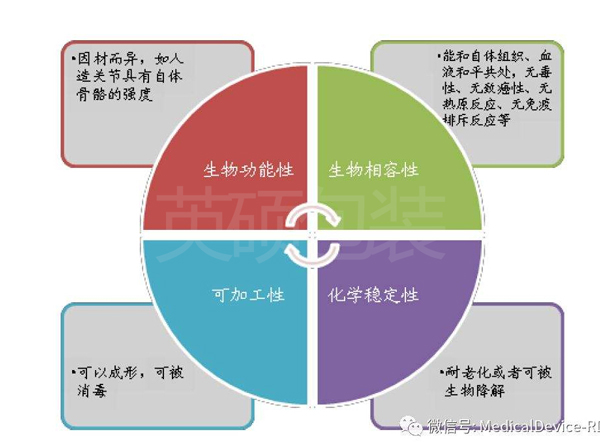
3. 物理和化学性能要求
常见的物理性能如:透气性能、抗张强度、厚度、微粒污染等;
常见的化学性能如:溶出物、气味、PH、重金属等;

4. 成型与密封过程的适应性
比如吸塑盒在设计时应注意预留密封宽度的有效数值,确保剥离时的完整性与强度。
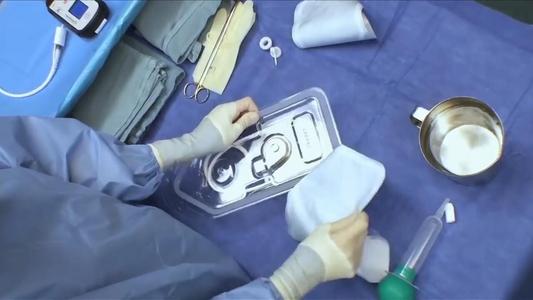
5. 与预期灭菌过程的适应性
包装材料的性能能否满足规定的灭菌方式(如灭菌方式、灭菌次数、灭菌条件)等

6. 灭菌前后的贮存寿命限度要求
应考虑包装材料无菌性维持能力,有效期内保持内包装材料的机械性能和化学性能的稳定性,维护完整的无菌屏障系统。
7. 毒性物质要求
在使用条件下,材料不论是在灭菌前、灭菌中、灭菌后应应不含有或者释放出有毒物质。

8. 涂胶材料要求
连续涂层,涂胶量符合标称要求,密封后应满足最终密封强度等。

9. 便捷/洁净开启性要求
无菌包装在保护产品维持无菌状态的前提下,还应便于洁净开启,过程当中保持剥离的连续完整性。这也要求到洁净开启的部位密封强度要适中。

10.印墨要求
标签印墨不应在包装材料上渗透迁移或反应,使用半包装上印黑要完整清晰。

11.对外在条件的敏感度要求
基于对医疗器械的贮存和运输,应考虑包装材料对温度、湿度、光线、氧、振动、压力等条件的敏感度。

文章综合自ISO11607《最终灭菌器械的包装》
文章出自专业医疗器械吸塑生产厂家——东莞市大岭山英硕塑胶制品厂(公司网址:www.yinsobz.com)转载请注明出处!
英硕包装专注医疗器械吸塑包装,致力于服务各大医疗器械厂家及医药制品公司。公司拥有ISO Class 万级洁净车间,全面通过ISO13485:2016。想要更进一步了解医用吸塑盒可致电:400-998-2901或0769-85602287。英硕包装将竭诚为您服务!
相关产品
热点资讯
- 英硕医用包装|新春开工启新程,安全护航再出发!2025-02-06
- 【英硕包装】2025 年春节放假通知2025-02-06
- 不同维度来了解医用吸塑盒与普通吸塑盒的差别2022-02-17
- 影响灭菌医疗器械包装环氧乙烷灭菌效果的因素2021-10-30
- 最终灭菌医疗器械包装常用系列标准参考2021-08-02
- 医用硬质吸塑盒的材质选择简述2021-07-20
- 无菌包装材料的评估项目及测试方法参考2021-07-17
- 影响医疗器械货架有效期的因素2021-07-17